Sin embargo, la colecta sin un fin lleva a que larvas no identificadas ocupen lugar en las colecciones aunque solo ocasionalmente serán identificadas para luego cumplir con algún estudio. Considerando el actual patrón de extinción de anfibios, y para sacrificio de larvas que no tendrán utilidad se recomienda que en el campo, al colectar larvas sin identidad específica separar un grupo para mantener vivo en el laboratorio (o en el campo) hasta la metamorfosis y allí proceder a la identificación. Un objetivo en la colecta de larvas es describir el estado larval si no ha sido reportado. En general es ideal describir el estado larval entre los estadios en los que se diferencian los dedos de las extremidades posteriores (Gosner 35–40), o sea una vez que las estructura larvales están completamente desarrolladas y antes que cambios metamórficos ocurran. Para estudios de anatomía esquelética se recomiendan descripciones entre estados 30 a 37, cuando el condrocráneo esta completamente desarrollado y la osificación no ha avanzado (en ambos casos las recomendaciones son estimaciones generales, debido a que estos patrones pueden variar a nivel genérico o específico).
Sacrificando:
Sobre anestesia en un medio acuoso con xilocaína, bezocaína. Inmediatamente traspasar al fijador.
Fijación para estudios convencionales:
Formol 10% (una parte de formol y 9 de agua común). No usar agua destilada o conviene bufferar la solución con carbonato de calcio o de magnesio. Para renacuajos grandes se puede agregar ácido acético puro al formol preparado (por ejemplo 15 ml de acético a 1 litro de formol 10%). El ácido acético actúa facilitando la penetración del formol en el renacuajo y así la fijación de partes internas es rápida.
Si no se ha podido lograr el desarrollo metamórfico de algunas larvas, es crítico fijar 2-3 larvas directamente en etanol 96%; al llegar al laboratorio cambiar el etanol por alcohol nuevo. Quizás este material permita identificarlas a través de análisis moleculares.
Posteriormente para identificación por medios moleculares, se retira parte de la cola para aislar ADN y el resto del ejemplar queda como “voucher” del material genético.
Un aspecto que se debe tener en cuenta es que en el campo, en lugares de altas temperaturas el formol 10 % se puede calentar y “quemar” al fijar las muestras, en estos casos el agregado de hielo es una buena forma para bajarle la temperatura. O simplemente se recomienda mantener el fijador en conservadora o refrigerador, a una menor temperatura.
El formaldehido de baja calidad o viejo precipita al poco tiempo; cuando en la botella se observe un precipitado blanco, no se debe ser usado para fijar nuestras muestras. Otra cosa que se debe evitar en el momento de fijar los renacuajos es hacerlo con plantas y barro.E
En el laboratorio, al identificar los renacuajos fijados y tomar los registros, se renueva el formol y se ubican en los recipientes apropiados. El formol neutralizado muchas veces es conveniente, con el tiempo tiende a acidificarse y puede modificar las estructuras de los tejidos. El volumen de fijador/conservante debe ser 10 veces el volumen de la muestra.
Fijación para estudios moleculares:
En los casos en los que se necesiten tejidos para identificación de la larva y/o estudios moleculares, genética y genómica fijar 2-4 renacuajos enteros (dependiendo del tamaño) en etanol 96% y el resto (larvas en diferentes estados de desarrollo) en formol 10%. También si es muy escaso el material see corta un pedacito de cola con una tijera muy limpia y se lo coloca directamente en un vial con etanol 96°. El resto del ejemplar queda como “voucher” del material genético.
Al regreso al laboratorio cambiar el etanol y el formol; la perdida de agua en tejidos durante la fijación diluye al agente fijador/conservante.
Sobre anestesia en un medio acuoso con xilocaína, bezocaína. Inmediatamente traspasar al fijador.
Fijación para estudios convencionales:
Formol 10% (una parte de formol y 9 de agua común). No usar agua destilada o conviene bufferar la solución con carbonato de calcio o de magnesio. Para renacuajos grandes se puede agregar ácido acético puro al formol preparado (por ejemplo 15 ml de acético a 1 litro de formol 10%). El ácido acético actúa facilitando la penetración del formol en el renacuajo y así la fijación de partes internas es rápida.
Si no se ha podido lograr el desarrollo metamórfico de algunas larvas, es crítico fijar 2-3 larvas directamente en etanol 96%; al llegar al laboratorio cambiar el etanol por alcohol nuevo. Quizás este material permita identificarlas a través de análisis moleculares.
Posteriormente para identificación por medios moleculares, se retira parte de la cola para aislar ADN y el resto del ejemplar queda como “voucher” del material genético.
Un aspecto que se debe tener en cuenta es que en el campo, en lugares de altas temperaturas el formol 10 % se puede calentar y “quemar” al fijar las muestras, en estos casos el agregado de hielo es una buena forma para bajarle la temperatura. O simplemente se recomienda mantener el fijador en conservadora o refrigerador, a una menor temperatura.
El formaldehido de baja calidad o viejo precipita al poco tiempo; cuando en la botella se observe un precipitado blanco, no se debe ser usado para fijar nuestras muestras. Otra cosa que se debe evitar en el momento de fijar los renacuajos es hacerlo con plantas y barro.E
En el laboratorio, al identificar los renacuajos fijados y tomar los registros, se renueva el formol y se ubican en los recipientes apropiados. El formol neutralizado muchas veces es conveniente, con el tiempo tiende a acidificarse y puede modificar las estructuras de los tejidos. El volumen de fijador/conservante debe ser 10 veces el volumen de la muestra.
Fijación para estudios moleculares:
En los casos en los que se necesiten tejidos para identificación de la larva y/o estudios moleculares, genética y genómica fijar 2-4 renacuajos enteros (dependiendo del tamaño) en etanol 96% y el resto (larvas en diferentes estados de desarrollo) en formol 10%. También si es muy escaso el material see corta un pedacito de cola con una tijera muy limpia y se lo coloca directamente en un vial con etanol 96°. El resto del ejemplar queda como “voucher” del material genético.
Al regreso al laboratorio cambiar el etanol y el formol; la perdida de agua en tejidos durante la fijación diluye al agente fijador/conservante.
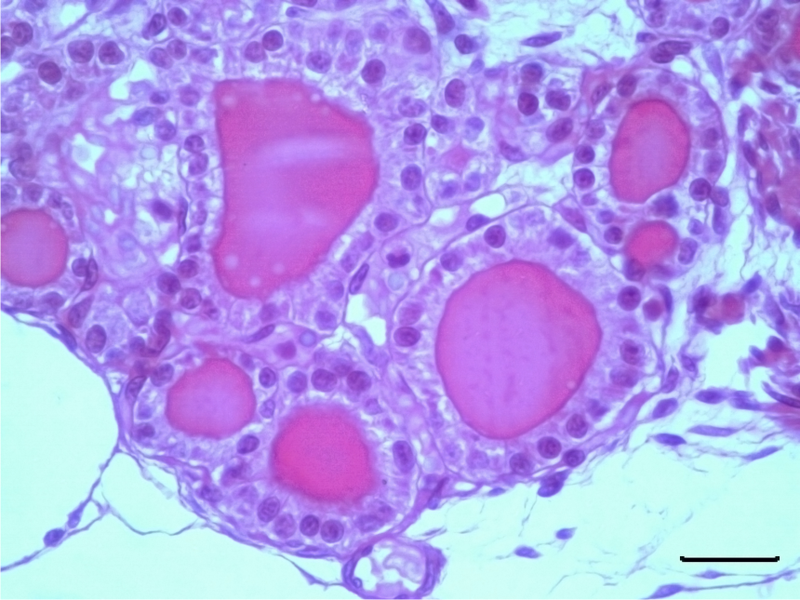
Fijación para estudios de microscopía
|
El fijador de Bouin demanda baja temperatura (no exponer al sol). Se usa directamente sobre el espécimen y el tiempo óptimo de fijación va entre 8 a 12 horas; si bien se puede dejar más tiempo dependiendo del tamaño de la muestra, recordar que no es un líquido de conservación por lo que luego de la fijación se debe transferir a alcohol 70° donde se conserva. Este fijador contiene ácido pícrico que con el tiempo forma cristalitos que pueden generar artefactos en las preparaciones histológicas. Se recomienda lavar bien con alcohol 70º para aclarar el tejido al momento de realizar histología.
En el caso de embriones con vitelo o larvas o simplemente tejidos que pretendan ser usadas para técnicas especiales como inmunolocalización o hibridación in situ, se puede usar paraformaldehído (al 4-8%) como fijador. El cual requiere una preparación compleja y bajo las medidas de seguridad adecuadas. Otro fijador es el glutaraldehído, muy usado para microscopía electrónica de transmisión (MET). Este fijador es usado entre el 1 al 3%, diluido en una solución buffer (pH 7.2-7.4). Presenta un muy bajo poder de penetración, razón por la cual los tejidos a fijar deben ser fragmentos de pocos milímetros cúbicos. Todo el proceso de disección y fragmentación del material se recomienda hacerlo en frío, por ejemplo en una capsula sumergida en hielo. Muchas veces es mejor trasladar los especímenes vivos hasta el laboratorio para trabajar con mayor comodidad. El glutaraldehído y el paraformaldehído también pueden ser usados como una mezcla diluida en buffer (fijador de Karnovsky) en la fijación de tejidos para MET.
En el caso de embriones con vitelo o larvas o simplemente tejidos que pretendan ser usadas para técnicas especiales como inmunolocalización o hibridación in situ, se puede usar paraformaldehído (al 4-8%) como fijador. El cual requiere una preparación compleja y bajo las medidas de seguridad adecuadas. Otro fijador es el glutaraldehído, muy usado para microscopía electrónica de transmisión (MET). Este fijador es usado entre el 1 al 3%, diluido en una solución buffer (pH 7.2-7.4). Presenta un muy bajo poder de penetración, razón por la cual los tejidos a fijar deben ser fragmentos de pocos milímetros cúbicos. Todo el proceso de disección y fragmentación del material se recomienda hacerlo en frío, por ejemplo en una capsula sumergida en hielo. Muchas veces es mejor trasladar los especímenes vivos hasta el laboratorio para trabajar con mayor comodidad. El glutaraldehído y el paraformaldehído también pueden ser usados como una mezcla diluida en buffer (fijador de Karnovsky) en la fijación de tejidos para MET.